강스템바이오텍, 골관절염 치료제 임상 1/2a상 IND 승인 단회투여·연골재생 신약개발 향해 ‘성큼’
세계 최초 골관절염 근본적 치료제 개발 위한 임상시험 진입
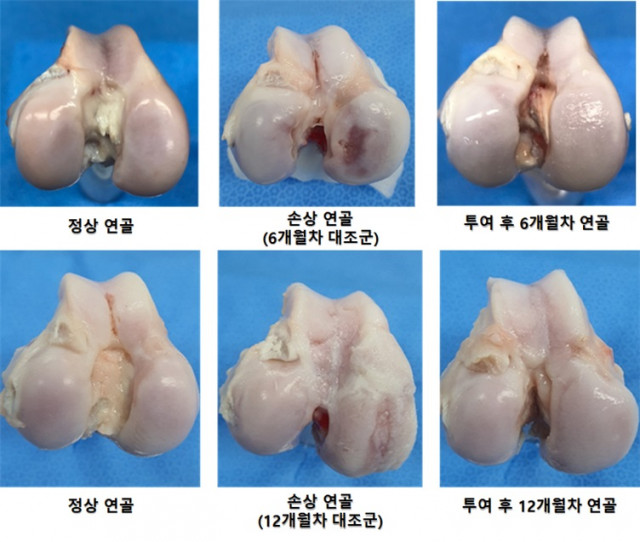
강스템바이오텍은 골관절염이 유발된 염소에 퓨어스템-오에이 키트주를 투여한 뒤 6개월, 12개월 시점에서 관절면의 구조개선을 평가한 결과로, 정상연골과 거의 동등한 수준으로 구조개선(연골조직 및 반월판 부위 재생, 염증 억제) 됨을 확인했다
서울--(뉴스와이어)--강스템바이오텍(대표 나종천)은 15일 줄기세포 기반 융복합제제 골관절염 치료제 ‘퓨어스템-오에이 키트주’의 임상 1/2a상을 위한 임상시험계획(IND)을 식품의약품안전처로부터 승인 받았다고 밝혔다.
퓨어스템-오에이 키트주는 제대혈 유래 중간엽줄기세포와 무세포성 연골기질을 함께 투여하는 융복합제제로, 세계 최초 골관절염 근본적 치료제(DMOAD)를 목표로 하고 있다. 특히 수술 없이 무릎관절강 내 주사 1회 투약만으로도 투여한 세포가 연골세포로 분화해 연골조직 재생에 직접적으로 기여함으로써 근본적인 치료 효과를 기대할 수 있다.
강스템바이오텍은 염소를 모델로 한 대동물시험에서 염증억제, 연골조직 및 반월판 부위 재생 등의 결과를 확보해 관절 통증완화와 함께 구조적 변형을 억제하거나 개선시킬 수 있는 치료제의 개발 가능성을 시사한 바 있다. 또한, 해당시험에서 투여된 세포가 재생조직 내에 6개월까지 잔존함을 확인해 퓨어스템-오에이 키트주의 차별화된 효능을 과학적으로 입증했다. 전임상시험에서 염소를 활용한 것은 무게 약 45~50kg으로 사람의 체중과 비교적 유사하고, 무릎을 많이 사용해 골관절염 유발 후 유효성을 평가하기에 적절하기 때문이다.
현재 골관절염 치료제 시장은 고령화 등으로 그 규모가 급격히 성장하고 있는 데 반해 일시적인 통증제어 수준의 치료제 또는 신체적 부담과 부작용이 우려되는 무릎절개술, 인공관절 삽입술과 같은 치료법에 의존하고 있는 상황이다. 이에 회사측은 향후 신약 개발 시 혁신적 치료제로서 시장 선점은 물론 환자들에게 획기적인 삶의 질 개선을 가능하게 할 것으로 기대된다고 전했다.
강스템바이오텍 나종천 대표는 “이번 임상시험에 해외 파트너사들의 관심이 집중돼 있다. 이미 국내를 비롯한 일본, 유럽에서 골관절염 치료제 관련 기술을 인정받아 특허를 취득해 향후 글로벌 사업화 및 기술이전을 위한 준비도 진행되고 있다”고 말했다. 이어 “특히 이번 IND 승인과정에서 강화된 첨단바이오의약품의 품목허가심사 규정에 부합하고자 세포은행을 구축해 품목허가 후 공급가 또한 큰 폭으로 줄일 수 있게 됐다”고 말했다.
한편 이번 임상시험은 ICRS(International Cartilage Repair Society, 연골결손 정도에 대한 국제표준기준) 3~4등급에 해당하는 중등증의 골관절염 환자를 대상으로, 무릎관절강 내 퓨어스템-오에이 키트주를 단회투여한 후 안전성 확보와 연골재생을 포함한 구조적 개선 및 통증관리의 유효성을 탐색한다.
임상 1상에서는 최대 18명의 골관절염 환자에게 저용량, 중용량, 고용량에 대한 내약성과 안전성을 확인할 예정이다. 임상 2a상은 총 50명의 골관절염 환자에게 안전성이 확인된 두 시험약 용량군의 6개월간 유효성을 위약군과 비교한다. 또한 장기추적조사와 연계해 12개월 시점에서의 유효성도 탐색할 계획이다.